
Perforar con aire comprimido continúa teniendo gran popularidad. Se utiliza, por lo general, para perforar en presencia de rocas duras, secas, ya que el fluido de perforación es poco costoso y, comparado con agua o lodo pesado de perforación, puede alcanzar respetables promedios de penetración.En términos de consideraciones económicas, con respecto a los gastos de fluidos de perforación, la perforación con aire no puede comprarse con ninguna. Sin embargo posee impedimentos como por ejemplo, su reacción con hidrocarburos.
PERSPECTIVA HISTÓRICA
El primer registro del uso del aire comprimido en la perforación es de 1860, cuando un trepano mecánico, de tipo pistón, perforó un túnel de 8 millas de longitud en los Alpes.
En 1940 y primeros del 50, la perforación con aire se volvió una solución importante a la perforación rotatoria standard
CONDICIONES DE SEGURIDAD
La perforación con aire comprimido provee muchos beneficios, pero una mala operación puede llevar a la pérdida equipos de superficie y de fondo del pozo, incluyendo daños al personal del equipo de perforación que en muchos casos pueden ser mortales.
La perforación con aire comprimido es segura siempre que las leyes de la naturaleza no sean violadas. Durante mucho tiempo operadores y contratistas de perforación y el personal del equipo, han tenido la equivocada impresión de que se trata de una operación más segura que la perforación convencional, sobre un amplio rango de aplicaciones.
Esto puede ser verdad, pero el concepto químico fundamental del triángulo de fuego ha sido muchas veces ignorado, descartado, u olvidado.
En 1952 fue publicada la cuarta edición de los estudios de inflamabilidad, llevados a cabo conjuntamente, por el Departamento del Interior de los EEUU, el Bureau de Minas, y el Consejo de Investigación de Seguridad en Minas de Gran Bretaña. En esta se describen los riesgos de trabajar en ambientes ricos en oxígeno, en presencia de hidrocarburos. Mientras no sean encontrados los hidrocarburos, la perforación con aire puede ser tan segura como la perforación con fluidos no reactivos, como agua, lodo a base de agua, lodo a base de petróleo, o de base sintética.El fuego es un proceso oxidante, la combustión solo se produce cuando se encuentran presentes las tres condiciones del triángulo clásico de combustión.
CLICKEAR SOBRE LA IMAGEN PARA AMPLIAR 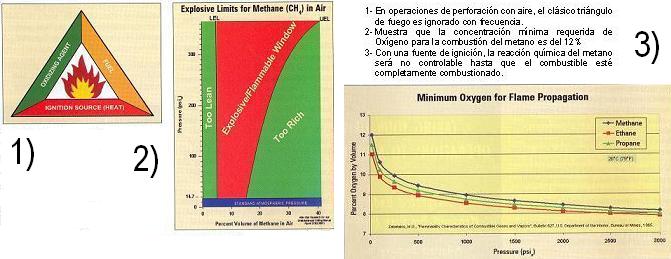
QUÍMICA
El aire es una mezcla de diferentes gases. Dentro de esa mezcla existe un 21 % de oxígeno. Sin embargo, el mínimo de concentración de oxígeno necesario para la combustión del metano es solo del 12 % al nivel del mar.El principal elemento constitutivo del gas natural es el metano (CH1). En presencia de una fuente de ignición, las reacciones químicas se producen según se describe más abajo:Cuando el agente oxidante (oxigeno) está presente en exceso:CH4 (gas) + 2 O2 (gas) „³ CO2 (gas) + H2O (liq) + calor (1)Con presencia de oxígeno suficiente, la combustión completa del hidrocarburo produce dióxido de carbono, más agua, más calor.
Cuando el combustible está en excesoCH4 (gas) + O2 (gas) „³ C (solidó) + H2O (Liq) + calor (2)Cuando hay un exceso de combustible o poco oxigeno, la reacción química no puede oxidar completamente las hidrocarburos hasta volverlos dióxido de carbono y agua. La reacción que se produce da como resultado un humo negro conocido como hollín (como producto sólido), más agua y calor.
CONFIABILIDAD
Cuando encendemos un horno somos testigos de una reacción controlada entre metano y oxígeno en presencia de una fuente de ignición que no presenta peligro. En condiciones normales de operación el proveedor del servicio de gas natural regula el flujo y la presión del metano de uso doméstico. Mientras la válvula del horno regula el flujo de encendido/apagado y el flujo en general, la válvula y el quemador regulan la cantidad de metano que debe ser combustionado. Cada mecanismo común de combustión es estrictamente controlado. Usualmente los hidrocarburos están restringidos. Los ejemplos incluyen no solo la mecha del quemador, sino también la carburación e inyección del combustible.
EMISIÓN DE HIDROCARBUROS A LA SUPERFICIE.
Una liberación de gas natural de la boca de pozo a la atmósfera abierta, ya sea por accidente o por diseño, provee dos condiciones de las tres necesarias para la combustión, explosión o incendio.La ignición puede virtualmente provenir cualquier fuente capaz de crear una chispa, incluyendo a la electricidad estática. El potencial de incidentes catastróficos aumenta porque este tipo de reacción es no controlable.
Hay una cantidad desconocida de metano y otros hidrocarburos en el pozo, la presión con frecuencia se desconoce, la cantidad liberada de hidrocarburos que fluyen del fondo es también desconocida, sin importar el esfuerzo siempre parece estar presente una potencial fuente de ignición.Si el metano liberado desde el pozo es altamente concentrado, eventualmente será dispersado en el aire para volverse un material potencialmente volátil, explosivo y combustible.En presencia de una fuente de ignición, la naturaleza explosiva de esta reacción química será no controlable hasta que el combustible este completamente combustionado. (Ecuación 1, fig. 3).
Las mezclas de aire e hidrocarburos tienen una velocidad de quemado máxima cuando la concentración del combustible es ligeramente menor que en el estequiométrico.
La mayoría de las explosiones y fuego en el fondo del pozo probablemente resulten de detonaciones en el fondo del pozo. Cuando el aire comprimido se expande, la expansión adiabática hacia la atmósfera produce un efecto de enfriamiento localizado. Cuando el aire atmosférico es comprimido la temperatura local aumenta por la compresión de las moléculas de aire en un espacio confinado. Esto se conoce como compresión adiabática.
Un mecanismo típico ocurre de la siguiente forma (Fig. 4)
CLICKEAR SOBRE LAS IMAGENES PARA AMPLIAR 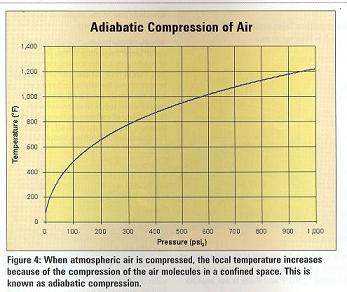
4)Cuando el aire atmosférico está comprimido, la temperatura local aumenta por la compresión de las moléculas de aire en un espacio confinado. Esto se conoce como “compresión adiabática”
5)La figura ilustra las temperaturas de 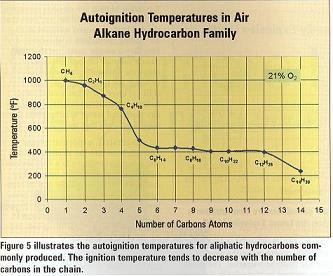 autoignicion para hidrocarburos alifáticos. La temperatura de ignición tiende a descender con el número de carbonos en la cadena
autoignicion para hidrocarburos alifáticos. La temperatura de ignición tiende a descender con el número de carbonos en la cadena
La sobrepresión creada durante una explosión, depende de la capacidad del frente de llamas para acelerarse y alcanzar altas velocidades. Los obstáculos y equipamientos en el interior del pozo son los principales contribuyentes a la aceleración de la llama.
La turbulencia inducida por los obstáculos en el camino de las llamas aumenta la velocidad creando una situación en la que la incrementada velocidad del fuego intensifica la turbulencia.Las altas velocidades de quemado crean altas sobrepresiones. En algunos casos, la explosión es tan intensa y tan violenta que puede hacer colapsar (literalmente) y doblar las tuberías de perforación.A veces no es necesario utilizar contenedores de desperdicios luego de una detonación, ya que los ensambles y el trepano en el fondo del pozo se desintegran debido a la sobrepresion de la explosión y la intensidad de la temperatura.
La detonación en el fondo del pozo parece ocurrir con más frecuencia en presencia de condensantes, también conocidos como gas húmedo. La figura 5 ilustra los tiempos de autoignicion comúnmente producidos para hidrocarburos alifáticos. La temperatura de ignición tiende a descender con el número de carbonos en la cadena. Un aumento en la presión típicamente reduce la temperatura espontánea de ignición.

6)Perforar en presencia de gas “seco” es aceptable mientras la Temperatura de compresión adiabática y la Temperatura estática del fondo del pozo, combinadas, no excedan los 1000 º F y no haya otra fuente de ignición.
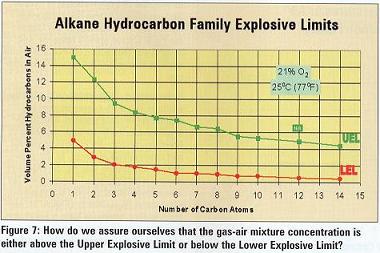
7)¿Como nos aseguramos que la mezcla de aire-gas se encuentra por encima o debajo de los Límites de Explosión?
2754 lecturas |
Ver más notas de la sección Novedad TĂ©cnica

 - BRENT 87,29
- BRENT 87,29  | DIVISAS: DOLAR 892,00 - EURO: 977,00 - REAL: 180,20 | MINERALES: ORO 2.361,45 - PLATA: 27,73 - COBRE: 445,00
| DIVISAS: DOLAR 892,00 - EURO: 977,00 - REAL: 180,20 | MINERALES: ORO 2.361,45 - PLATA: 27,73 - COBRE: 445,00 






